Glossar
Absolute Risikoreduktion
Erinnern Sie sich an das Beispiel?
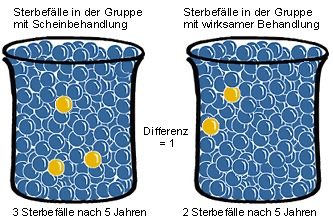
Erhalten 1000 Personen einer Gruppe dieselbe wirksame Behandlung, versterben innerhalb von 5 Jahren 2. Von 1000 Personen ohne Behandlung versterben im gleichen Zeitraum 3.
Vergleicht man die Zahlen der Verstorbenen in den beiden Gruppen, so ist es in der behandelten Gruppe eine Person weniger. Bezieht man diese Zahl von einer Person, auf die ge-
samte behandelte Gruppe von 1000 Personen, so sind 0,1% weniger gestorben. Die 0,1% sind die Absolute Risikoreduktion.
Absolutes Risiko
Das absolute Risiko bezeichnet die Ereignisrate in einer Gruppe.
Beispiel:
In einer Gruppe von 1000 Personen, die eine wirksame Behandlung erhalten sterben 2 Personen.
In einer Gruppe von 1000 Personen ohne Behandlung versterben im gleichen Zeitraum 3 Personen.
Das absolute Risiko zu versterben beträgt in der Behandlungsgruppe (2 auf 1000) oder 0,2 % und in der Kontrollgruppe (3 auf 1000) oder 0,3%.
BIAS
Ein Bias ist ein systematischer Fehler, der zur Verzerrung von Studienergebnissen führt. Man unterscheidet verschiedene Formen eines Bias:
Selektionsbias: Durch eine ungewollte Selektion von Patienten können bereits bei Studienbeginn systematische Unterschiede zwischen den Gruppen, die miteinander verglichen werden sollen, entstehen. So kann ein Unterschied im Ergebnis lediglich darauf beruhen, dass in der einen Gruppe z.B. Patienten mit schwereren Erkrankungsformen oder ausgeprägterem Risikoprofil beobachtet wurden. Der gemessene Unterschied ist dann lediglich ein scheinbarer Unterschied.
Performance Bias: Gewisse Patienten erhalten im Rahmen einer Studie eine bessere medizinische Versorgung, werden engmaschiger überwacht oder zusätzlich unterstützt. Ein Performance Bias kann z.B. zu Stande kommen, wenn das Studienpersonal nicht verblindet ist und Patienten in einer Gruppe (bewusst oder unbewusst) eine bessere medizinische Versorgung bekommen.
Detection Bias: Gewisse Patienten werden im Rahmen einer Studie genauer untersucht und beobachtet hinsichtlich eines Outcomes. Ein Detection Bias kann z.B. zu Stande kommen, wenn das Studienpersonal nicht verblindet ist.
Publication Bias: Es werden nur Studien veröffentlicht, die einen positiven Effekt einer medizinischen Maßnahme nachweisen. Studien, die keinen Effekt dieser Maßnahme nachweisen, werden nicht publiziert. Dadurch entsteht ein unausgewogenes Bild über die Wirksamkeit einer Therapie.
Confounder
Confounder sind Störgrößen, die zu einer Ergebnisverfälschung führen. Ein Confounder ist selbst kein Risikofaktor für eine Erkrankung, ist aber mit einem Risikofaktor assoziiert.
Beispiel: Man findet eine Assoziation zwischen Kaffeetrinken und der Entwicklung einer koronaren Herzkranheit. Bei genauerer Betrachtung fällt aber auf, dass sich in der Gruppe der „Exponierten“ (= Kaffeetrinker) mehr Raucher befinden. Kaffeetrinken ist in diesem Beispiel ein Confounder: Es resultiert ein scheinbarer Zusammenhang mit der koronaren Herzkrankheit, weil Raucher oft Kaffee trinken und Rauchen einen echten Risikofaktor für die koronare Herzkrankheit darstellt.
Durch statistische Korrekturen kann die Ergebnisverfälschung durch einen Confounder beseitigt werden
Endpunkt (Zielkriterium)
Als primärer Endpunkt einer Studie ist derjenige Parameter festzulegen, der bezüglich der Hauptfragestellung die relevanteste Beantwortung ermöglicht.
Sekundäre Endpunkte sind weitere Parameter, die zusätzlich zu den primären Endpunkten erfasst werden und zur Beurteilung des Studienergebnisses von Bedeutung sind.
Follow-up
Für Studien muss bereits in der Planungsphase der Zeitrahmen, in dem Studienteilnehmer weiter beobachtet werden, festgelegt werden.
Dieses wird als Follow-up bezeichnet.
Funnel Plot
Darstellungsweise der Ergebnisse einer Meta-Analyse

Heterogenität
In systematischen Reviews oder Meta-Analysen bezeichnet Heterogenität, inwieweit die in den eingeschlossenen Studien gefundenen Effekte verschieden (heterogen) sind.
Mit statistischen Heterogenitätstests kann festgestellt werden, ob die Unterschiede zwischen den Studien größer sind, als zufallsbedingt zu erwarten wäre.
Als Ursachen für Heterogenität kommen Unterschiede in den Patientencharakteristika, Intervention oder Endpunkte zwischen den Studien in Frage.
Die Durchführung einer Meta-Analyse* aus heterogenen Studien ist problematisch.
Homogenität
In systematischen Reviews oder Meta-Analysen bezeichnet Homogenität inwieweit die in den eingeschlossenen Studien gefundenen Effekte ähnlich (homogen) sind.
Informed Consent
"Informed Consent" ist die auf der Grundlage einer ausführlichen Information erteilte Zustimmung eines Patienten zu einer diagnostischen oder therapeutischen Maßnahme. Die vorausgehende Aufklärung muss sicherstellen, dass der Patient in verständlicher Form über alle zu seiner bestimmten Fragestellung verfügbaren Möglichkeiten, deren Nutzen, Risiken und Nebenwirkungen beraten wird.
Die "informierte Zustimmung" (informed consent) als Voraussetzung medizinischer Interventionen zu therapeutischen oder Forschungszwecken ist international Standard.
Intention-To-Treat Analyse
Die Teilnehmer einer Studie werden in den Gruppen analysiert zu denen sie zu Studienbeginn zugeteilt wurden.
Inzidenz
Mit der Inzidenz wird die Anzahl neu aufgetretener Krankheiten in einem bestimmten Zeitraum be-schrieben. Meistens erfolgen die Angaben pro Jahr. Die Angabe der Neuerkrankungen erfolgt oft ge-trennt für verschiedene Gruppen, zum Beispiel Frauen, Männer oder für verschiedene Alters-gruppen.
Ein Beispiel:
1994 betrug die Krebsinzidenz in Hamburg etwa 446 Neuerkrankungen pro 100.000 Einwohner.
Konfidenzintervall (Vertrauensbereich)
Stellen Sie sich bitte vor, Sie haben sich mit Freunden am Michel verabredet. Ihre Freunde sind nicht aus Hamburg und fragen Sie, wie lange man für die Busfahrt zum Michel benötigt. Sie können Ihnen sagen, dass man ungefähr 20 Minuten benötigt. Vor dem Berufsverkehr braucht man oft nur 15 Minuten. Ab 16:00 nachmittags in der Woche sollte man allerdings 30 Minuten einplanen. Die Spanne zwischen 15 und 30 Minuten stellt den Vertrauensbereich dar. Darin liegt der wahre Wert.
Häufig wird ein 95% Konfidenzintervall angegeben, das heißt, der wahre Wert liegt mit 95%iger Sicherheit im angegebenen Intervall.
Auch bei der Darstellung medizinischer Daten treffen Sie auf Konfidenzintervalle.
Je größer die untersuchte Gruppe, umso präziser sind die Schätzwerte, das bedeutet auch, dass die Konfidenzintervalle enger werden.
Number Needed to Treat (NNT)
Die Number Needed to Treat ist die Anzahl an Patienten, die behandelt werden muss, um ein Ereignis z.B. Tod, Herzinfarkt oder anderes zu verhindern.
Wenn ein Medikament eine NNT von 5 hat, bedeutet das, dass 5 Personen behandelt werden müssen, um z.B. ein Ereignis zu verhindern.
Berechnung der NNT: NNT= 1/Absolute Risikoreduktion
Prävalenz
Mit der Prävalenz wird die Anzahl von Personen beschrieben, die zu einem bestimmten Zeitpunkt (Punktprävalenz) an einer Krankheit erkrankt sind. Aufgrund fehlender Daten liegen häufig nur Schätzungen für Prävalenzen vor.
P-Wert
Die statistische Signifikanz (p-Wert) sagt aus, wie groß die Wahrscheinlichkeit ist, dass der gemessene Unterschied zwischen den beiden Studiengruppen zufällig zustande gekommen ist.
P< 0.05 bedeutet, dass die Wahrscheinlichkeit kleiner als 5% ist, dass der gemessene Unterschied zwischen den zwei Vergleichsgruppen (z.B. 1% weniger Lungenkrebs in der Gruppe 1 als in der Gruppe 2) nur auf Zufall beruht.
Wenn die untersuchten Gruppen genügend groß sind, erlangen schon kleine Unterschiede zwischen zwei Gruppen statistische Signifikanz. Der p-Wert ist ein rein statistischer Ausdruck und sagt nichts aus über die klinische Bedeutung des Ergebnisses.
Präzision eines Tests

Alle drei Versuche treffen ins Schwarze. Damit ist die Präzision des Tests sehr gut. Der Test ist präzise.
Drei Versuche führen zudem zu gleichen Ergebnissen. Das heißt, die Treffsicherheit des Tests ist ebenfalls sehr gut.
Dieser Test wäre ideal.
Relative Risikoreduktion
Erinnern Sie sich an das Beispiel?
Erhalten 1000 Personen einer Gruppe dieselbe wirksame Behandlung, versterben innerhalb von 5 Jahren 2.
Von 1000 Personen ohne Behandlung versterben im gleichen Zeitraum 3.
Vergleicht man die Zahlen der Verstorbenen in den beiden Gruppen, so ist es in der behandelten Gruppe eine Person weniger. Bezieht man diese eine Person auf die 3, so ergeben sich 30%.
Also 30% weniger in der behandelten Gruppe.
Die Relative Risikoreduktion beschreibt also den Unterschied zwischen 2 Gruppen.

Relatives Risiko
Das relative Risiko setzt das Erkrankungsrisiko (z.B. bei Lungenkrebs) von Risikopatienten (z.B. Rauchern) in Beziehung zu dem Risiko von Nichtrauchern, an Lungenkrebs zu erkranken.
Beispiel:
Die Todesrate von Lungenkrebs pro 100 000 Einwohner beträgt für Raucher 140 und für Nichtraucher 10.
Damit beträgt das RR 140/10 = 14,0 (Todesfälle pro 100 000 Einwohner)
Sensitivität
Die Sensitivität eines diagnostischen Tests beschreibt seine Fähigkeit, Kranke als krank zu erkennen, also positiv zu testen. Die Sensitivität beschreibt den Anteil der erkrankten Personen einer Gruppe, die durch einen Test aus der Gesamtzahl der Erkrankten richtigerweise entdeckt werden.
Das Bild zeigt 100 Punkte = 100 Personen. Die hellen Punkte stellen die Gesunden, die schwarzen Punkte die kranken dar. Wenn Sie jetzt die Gruppe der Erkrankten betrachten (linker Kasten), sehen Sie, dass 24 rot unterlegt sind. Diese wurden auch als krank erkannt, d.h. positiv getestet. 6 sind grün unterlegt. Diese 6 wurden übersehen, d.h. negativ getestet.
Berechnung: Positiv Getestete, die tatsächlich erkrankt sind / Gesamtzahl der Erkrankten. Die Angabe erfolgt in Prozent.
Im Beispiel 24 / 30 = 0,8 x 100 = 80%

● Kranke
o Gesunde
rot unterlegt = positiv getestet
grün unterlegt = negativ getestet
Signifikanz
Stellen Sie sich vor, Sie würden zwei Gruppen Ihrer Patienten unterschiedlich behandeln. Später würden Sie diese untersuchen, die Ergebnisse miteinander vergleichen und einen Unterschied feststellen.
Ob der Unterschied auf einem Zufall beruht oder nicht, das beschreibt der p-Wert. Der Buchstabe p steht für "probability" und bedeutet Wahrscheinlichkeit Je kleiner der p-Wert desto größer die "statistische Signifikanz". Daraus können dann Schlüsse gezogen werden über den Einfluss der unterschiedlichen Behandlungen auf das Ergebnis.
Ab welchem p-Wert wird nun ein Unterschied als statistisch signifikant inter-pretiert? Willkürlich wurde die Entscheidung getroffen, dass die Grenze zwischen einem signifikanten und nicht signifikanten Wert in der Medizin (meist) bei 0,05 liegt.
Das bedeutet, dass bei einem p-Wert von 0,05 oder darüber der Unterschied nicht statistisch signifikant ist.
Spezifität
Die Spezifität eines diagnostischen Tests beschreibt seine Fähigkeit, Gesunde als gesund zu erkennen. Die Spezifität beschreibt den Anteil der gesunden Personen einer Gruppe, die durch einen Test aus der Gesamtzahl der Gesunden richtigerweise als nicht erkrankt erkannt werden.
Das Bild zeigt 100 Punkte = 100 Personen. Die hellen Punkte stellen die Gesunden, die schwarzen Punkte die kranken dar. Wenn Sie jetzt die Gruppe der Gesunden betrachten (linker Kasten), sehen Sie, dass 56 grün unterlegt sind. Diese wurden auch als gesund erkannt, d.h. negativ getestet. 14 sind rot unterlegt. Diese 14 wurden fälschlicherweise positiv getestet.
Berechnung: Negativ Getestete, die tatsächlich gesund sind / Gesamtzahl der Gesunden. Die Angabe erfolgt in Prozent. Im Beispiel 56 / 70 = 0,8 x 100 = 80%

● Kranke
o Gesunde
rot unterlegt = positiv getestet
grün unterlegt = negativ getestet
Stichprobengröße
Unter einer Stichprobe versteht man die Gruppe der Untersuchten / Befragten.
Diese sollen einen Ausschnitt einer bestimmten Gesamtheit repräsentieren, und müssen daher in allen Eigenschaften ein möglichst charakteristisches Bild dieser Gesamtheit liefern.
Die Abschätzung der Stichprobengröße für eine Studie ist deswegen von Bedeutung, weil zu große Stichproben eine unnötige Verschwendung von Geldern bedeuten, während eine zu kleine Stichprobe die Ergebnisse fragwürdig werden lässt.
Surrogatparameter
In manchen Studien werden keine bedeutsamen Ereignisse (wie zB Schlaganfall oder Tod), sondern so genannte Surrogatparameter beschrieben.
Surrogatparameter stellen „Ersatzmessgrößen“ dar, die zwar mit dem Risiko für das Auftreten eines solchen bedeutsamen Ereignisses in Verbindung gebracht werden, aber keine sichere Aussage bezüglich dieses Ereignisses (auch: klinischer Endpunkt) erlauben und deshalb zu Trugschlüssen führen.
Gute Studien sollten Endpunkte untersuchen, die medizinisch gewichtig und auch für den Patienten relevant sind.
Dazu gehören Sterblichkeit, Lebensqualität u.a.
Beispiel:
In Studien zur Messung der Wirkung von Medikamenten gegen Bluthochdruck wäre ein echter klinischer Endpunkt eine schwere Erkrankung wie z.B. ein Schlaganfall oder der Tod, während ein Surrogatparameter den Blutdruck beobachtet.
Treffsicherheit

Beispiel A:
Drei Versuche (wiederholte Messungen in einem Test) führen zu sehr ähnlichen Ergebnissen. Diese Eigenschaft der Wiederholbarkeit wird als Treffsicherheit bezeichnet. Dieser Test hat eine hohe Treffsicherheit.

Beispiel B:
Drei Versuche führen zu sehr unterschiedlichen Ergebnissen. Das heißt, die Wiederholbarkeit ist schlecht.
Dieser Test hat keine hohe Treffsicherheit.
Vorhersagewerte
Positiver Vorhersagewert (positiv-prädiktiver Wert)
Der positive Vorhersagewert (positiv-prädiktive Wert - PPW) beschreibt bei diagnostischen Tests und Früherkennungstests den Anteil der Personen mit positivem Testergebnis, die tatsächlich die Erkrankung aufweisen.
Berechnung: Personen mit positivem Testergebnis / Gesamtzahl der positiv Getesteten
Negativer Vorhersagewert (negativ-prädiktiver Wert)
Der negative Vorhersagewert (negativ prädiktiver Wert - NPW) beschreibt bei diagnostischen Tests und Früherkennungstests den Anteil der Personen mit negativem Testergebnis, die tatsächlich die Erkrankung nicht aufweisen.
Berechnung: Personen mit negativem Testergebnis / Gesamtzahl der negativ Getesteten
